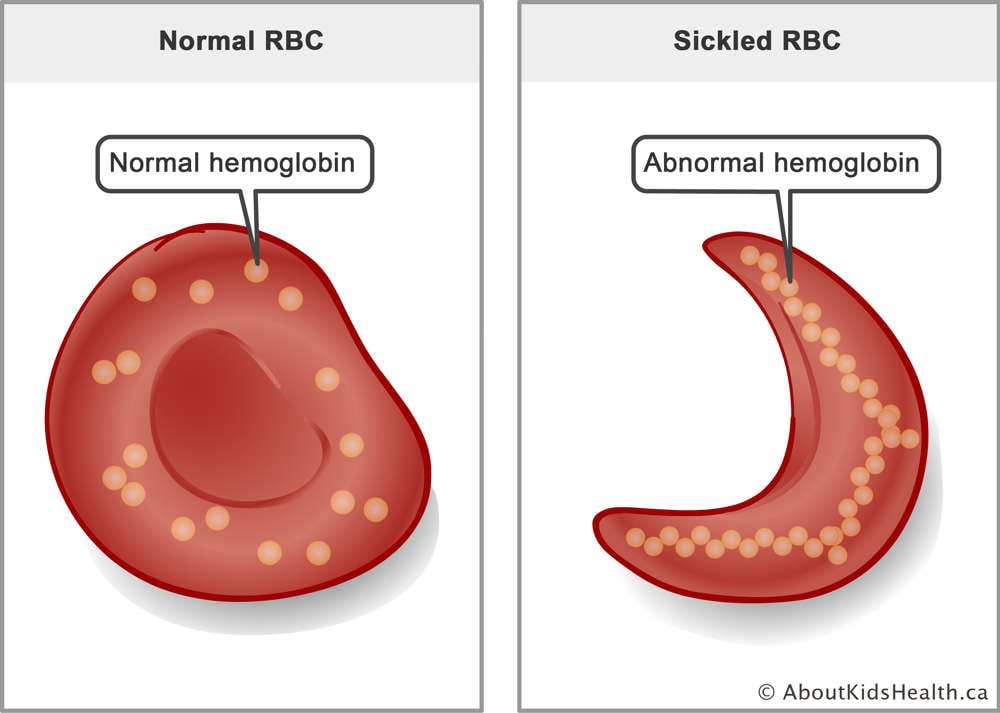
Si bien algunos fabricantes de vacunas están utilizando nuevos enfoques para combatir el COVID-19, otros están recurriendo a métodos más establecidos para poner fin a la pandemia.
AstraZeneca y la Universidad de Oxford han estado trabajando en una vacuna basada en adenovirus, oficialmente llamada ChAdOx1 nCoV-19 (AZD1222). La vacuna es una vacuna de vector viral. Esto significa que usa un adenovirus—Un virus que causa el resfriado común— para transportar material genético del virus SARS-CoV-2.
Los científicos pudieron desarrollar la vacuna rápidamente ya que esta tecnología de vacuna ha existido durante décadas.
Oxford había estado estudiando vacunas basadas en adenovirus para varias otras enfermedades como el virus Zika cuando surgió COVID-19. Los investigadores utilizaron un adenovirus de chimpancé debilitado para desarrollar la vacuna. Un ensayo de Fase 1 comenzó en abril de 2020, con más de 1,000 vacunas administradas en el Reino Unido.
Los resultados iniciales del ensayo de fase 3 se publicaron a principios de diciembre e investigaron qué tan bien funcionó la vacuna en más de 11,000 personas mayores de 18 años inscritas en cuatro grupos de ensayo en el Reino Unido, Brasil y Sudáfrica.
Ha habido cierta controversia en torno a esta vacuna, que incluye:
-
Discrepancias de dosificación en algunos grupos de estudio
-
Complicaciones inexplicables que llevaron a la Administración de Alimentos y Medicamentos (FDA) a pausar el ensayo en EE. UU. (Sin embargo, la FDA reinició el ensayo después de revisar los datos de seguridad)
-
Posible vínculo con los coágulos de sangre que da como resultado aproximadamente una docena de países europeos que habían autorizado la vacuna para pausar las vacunas temporalmente.
Después de una revisión, la Agencia Europea de Medicamentos (EMA) anunció el 18 de marzo de 2021 que no encontró un aumento general del riesgo de coágulos sanguíneos. Sin embargo, encontró una posible asociación con un tipo de coágulo sanguíneo muy raro.
La EMA concluyó que los beneficios de la vacuna aún superan los riesgos de posibles efectos secundarios, especialmente considerando que COVID-19 también puede provocar coágulos de sangre. La Organización Mundial de la Salud (OMS) también emitió un comunicado instando a los países a continuar con la vacunación.
Aún no hay audiencias programadas sobre una autorización de uso de emergencia por parte de la FDA. Sin embargo, se espera que el ensayo clínico de EE. UU. Dure hasta septiembre de 2021.
Este artículo explica cómo funciona la vacuna AstraZeneca-Oxford, su efectividad, disponibilidad, efectos secundarios y quién es elegible para recibir la vacuna.
:max_bytes(150000):strip_icc()/GettyImages-1227138063-d164a147499449c295e2ea44a672e2f4.jpg)
Cómo funciona
La vacuna AstraZeneca-Oxford es una recombinante vacuna de vector adenoviral. Las vacunas recombinantes utilizan una pequeña pieza de material genético de un patógeno (organismo infeccioso), como el SARS-CoV-2, para desencadenar una respuesta inmunitaria. De esta forma, la vacuna puede apuntar a una parte específica del virus.
Las vacunas recombinantes generalmente son seguras de usar en una gran población de personas, incluso aquellas con problemas de salud crónicos o personas con sistemas inmunológicos debilitados.
La vacuna AstraZeneca-Oxford utiliza un patógeno vivo debilitado. Un inconveniente de las vacunas de vectores adenovirales recombinantes es que las personas pueden requerir inyecciones de refuerzo con el tiempo.
Ejemplos de tipos similares de vacunas recombinantes (que no usan patógenos vivos) son:
- Vacunas antineumocócicas
- Vacunas antimeningocócicas
Si bien las vacunas recombinantes son comunes, la única vacuna de este tipo basada en adenovirus disponible comercialmente es una vacuna contra la rabia para animales.
Dado que los adenovirus son tan comunes en el medio ambiente, las vacunas contra adenovirus pueden plantear algunos problemas, que incluyen:
- Es posible que las dosis de refuerzo de la vacuna no sean tan efectivas.
- Es posible que algunas personas ya tengan inmunidad al virus que se usa en la vacuna.
Dosificación
Los investigadores probaron la vacuna AstraZeneca-Oxford usando dos dosis administradas con un mes de diferencia. La dosis utilizada en los ensayos no está clara. El servicio de noticias Reuters descubrió por primera vez diferentes versiones de los cambios de dosis.
AstraZeneca y Oxford dieron a los reporteros de la agencia de noticias dos respuestas diferentes sobre si un subgrupo en el brazo del estudio del Reino Unido recibió medias dosis de la vacuna a propósito o por accidente. Los reporteros descubrieron la discrepancia después de que se publicaron los resultados preliminares.
¿Qué tan efectivo es?
Ya sea por accidente o intencionalmente, el cambio de dosis parece haber sido afortunado.
Según el informe del ensayo, la serie de dos dosis de la vacuna AstraZeneca-Oxford tiene una efectividad de aproximadamente un 70%, en promedio. Sin embargo, los investigadores calcularon este promedio después de encontrar una tasa efectiva del 62% en las personas que recibieron la dosis completa de la vacuna en su primera inyección, en comparación con el 90% de efectividad en las que recibieron la mitad de la dosis.
Se están realizando revisiones adicionales. No está claro en este momento por qué una media dosis de vacuna podría haber funcionado mejor que una primera dosis completa.
Según estudios limitados, se ha demostrado que la vacuna también brinda protección contra la variante Delta (B.1.617.2). Un estudio publicado en The New England Journal of Medicine encontró que una dosis de la vacuna AstraZeneca-Oxford tiene un 30% de efectividad contra esta variante y dos dosis tienen un 67% de efectividad.
¿Cuándo estará disponible?
La disponibilidad depende de dónde viva.
Europa
La vacuna está ampliamente autorizada en Europa para su uso en adultos mayores de 18 años. Esta autorización es a pesar de los argumentos iniciales sobre la dosificación y las pausas temporales tanto en los ensayos como en las vacunas.
La compañía anunció en noviembre de 2020 que aún se están realizando pruebas en todo el mundo. Pero, en espera de aprobaciones regulatorias, hasta 3 mil millones de dosis podrían estar disponibles en 2021.
La vacuna puede ser más fácil de distribuir que otras opciones de vacuna COVID-19. Esto se debe a que, en lugar de requerir temperaturas de almacenamiento extremadamente frías como algunas otras vacunas, la vacuna AstraZeneca-Oxford solo necesita refrigeración estándar. Además, se estima que cuesta solo entre $ 3 y $ 4 por dosis.
nosotros
Si y cuándo la vacuna AstraZeneca-Oxford podría estar disponible en los Estados Unidos es una gran pregunta. Los Centros para el Control y la Prevención de Enfermedades (CDC) lideran los esfuerzos de vacunación, y todos los pedidos de la vacuna COVID-19, independientemente del fabricante, pasarán por la agencia.
Los CDC también supervisan la distribución de vacunas. Además, el Comité Asesor de Prácticas de Inmunización (ACIP) de los CDC ha hecho recomendaciones sobre la priorización de los suministros de vacunas.
Los trabajadores de la salud y las personas que viven en centros de atención a largo plazo fueron los grupos prioritarios para recibir las vacunas COVID-19 autorizadas. Ahora, la vacuna está disponible y se recomienda para todas las personas mayores de 12 años, y también se espera autorización para los niños.
Solo Estados Unidos tiene una población de aproximadamente 330 millones. Hasta ahora, otras opciones de vacunas están satisfaciendo la demanda.
Vacunas COVID-19: Manténgase actualizado sobre las vacunas disponibles, quién puede recibirlas y qué tan seguras son.
¿Quién puede recibir la vacuna AstraZeneca?
El ensayo clínico inicial de la vacuna AstraZeneca-Oxford se centró en personas de 18 a 55 años. Los nuevos ensayos con personas mayores de 55 años comenzaron en agosto de 2020.
Hubo ensayos iniciales con niños, pero los investigadores eliminaron a ese grupo de los datos del ensayo a mediados de diciembre de 2020. AstraZeneca y Oxford no han hecho ninguna declaración sobre el cambio.
En febrero de 2021, la Universidad de Oxford anunció el lanzamiento de una nueva prueba para niños que inscribirá a 300 participantes de entre 6 y 17 años.
Efectos secundarios y eventos adversos
Generalmente, los efectos secundarios de las vacunas COVID-19 han incluido reacciones menores que son típicas de la mayoría de las vacunas. Estos han incluido cosas como:
- Dolor en el brazo
- Hinchazón del brazo
- Enrojecimiento en el lugar de la inyección.
Se han informado algunos otros efectos adversos, incluido uno que provocó una pausa en el ensayo clínico AstraZeneca-Oxford.
Eventos adversos frente a efectos secundarios
Un efecto secundario es una respuesta física a un medicamento, mientras que un evento adverso es una reacción más importante desde el punto de vista médico y menos común relacionada con el medicamento.
El informe preliminar sobre la vacuna publicado en The Lancet reveló resultados generalmente buenos en términos de efectos secundarios. Pero hubo algunas reacciones adversas preocupantes.
Hubo tres casos de mielitis transversa, una afección en la que hay inflamación de la médula espinal, en personas que recibieron la vacuna. Sin embargo, según el informe del ensayo, es poco probable que estas enfermedades hayan sido causadas por la vacuna.
También se informaron algunas muertes en el estudio (la mayoría en el grupo de control). Pero esas muertes no estaban relacionadas con la vacuna y se debieron a incidentes como accidentes de tránsito y homicidios.
Financiamiento y desarrollo
Los científicos desarrollaron la vacuna a través de una asociación entre Oxford y AstraZeneca. El apoyo financiero para el estudio también fue proporcionado por:
- Reino Unido Investigación e Innovación
- La Fundación Bill y Melinda Gates
- El Centro de Investigación Biomédica de Oxford NIHR
- Red de investigación clínica de los NIHR de Thames Valley y South Midland
La información de este artículo está actualizada a la fecha indicada, lo que significa que puede haber información más reciente disponible cuando lea esto. Para obtener las actualizaciones más recientes sobre COVID-19, visite nuestra página de noticias sobre coronavirus.